2022-11-19今日SH688505股票最新净值和交易情况
复旦张江(SH688505):
复旦张江:H股公告 网页链接
复旦张江(SH688505):
复旦张江:H股公告 网页链接
滴滴哈哈43o:
21世纪经济报道记者 季媛媛 实习生 洪小澜 上海报道
复旦张江(SH688505)百奥泰(SH688177)君实生物-U(SH688180)
近日,国家药品监督管理局药品审评中心(CDE)再度发布《抗肿瘤抗体偶联药物临床研发技术指导原则(征求意见稿)》(以下简称《指导原则》)指出,生物制药技术的发展推动抗体偶联药物(ADC)进入高速发展阶段,使之成为目前抗肿瘤新药研发热点之一。尤其在肿瘤治疗领域,ADC的研发持续增长,正在引领一个新的靶向治疗新时代。该《指导原则》旨在对ADC 类抗肿瘤药物的临床研发中需要特殊关注的问题提出建议。
《指导原则》提出,临床研发应关注同一靶抗原不同药物间疗效差异、最佳给药方案探索等要点。此外,随着科技进步,后续将不断有新的ADC产品被开发运用到临床试验中,如双表位或双靶点ADC等。但可预期的是,与目前已有ADC药物一样,其每一个组成部分都可能会直接影响产品的安全性和有效性。
瓴路药业联合创始人兼首席执行官张晓雷在接受21世纪经济报道记者采访时表示,该《指导原则》的意义在于,从政策层面,国家希望在ADC市场布局上,企业要借助前沿技术平台,聚焦“护城河比较宽,城墙比较高”的适应症领域。《指导原则》的提出也要求在ADC这一赛道的入局企业要将战略价值作为长期考虑的方向。作为ADC企业布局者一定要借助前沿技术瞄准差异化靶点,切勿扎堆布局热门适应症。
“一方面,在技术平台应用上,要综合考虑毒素、Linker、是否能增加治疗窗口、毒性是否较小、疗效是否能有所提升、治疗周期是否能缩短等方面;另一方面,在靶点选择上,Her2已经遍地开花,将来或成为下一个PD-1,这可能会对患者资源、医疗资源造成一定浪费。所以,ADC赛道需要更多差异化靶点的布局。”张晓雷说。
ADC带来“新风口”
ADC 药物由靶向特异性抗原的抗体药物与有效载荷(如小分子细胞毒药物)通过连接子偶联而成,兼具传统小分子细胞毒药物的强大杀伤效应和抗体药物的肿瘤靶向性。开发 ADC 药物的主要目标是通过将有效载荷靶向递送到特定部位,以实现有效载荷的全身暴露相对较低,有效地提高抗肿瘤治疗的获益风险比。
由此,基于ADC相较于化疗药物毒性更可控,新一代ADC取得了显著优于化疗疗法的临床治疗数据。相较传统靶向疗法,ADC进一步拓宽了治疗人群,可应用于未被传统靶向疗法覆盖的新靶点。
这也催生不少ADC药物面市,并实现销量的迅速增长。IQVIA数据显示,2016年-2020年,美国ADC市场销售额从3.29亿美元增长至14.7亿美元,年均复合增长率高达45%。另据Nature子刊市场预测,到2026年,全球ADC药物市场规模将达到164亿美元。中信证券研报也显示,到2026年,全球ADC药物市场规模有望超过400亿美元。
不断超乎预期的临床成功,叠加庞大的市场空间,点燃了国内外药企的研发热情,使ADC成为创新药产业里最炙手可热的细分领域。仅2020年9月,就有两笔引人注目的交易,凸显出大制药公司对ADC领域的浓厚兴趣。其中,吉利德科学以约210亿美元收购Immunomedics,获得靶向Trop-2的first-in-class抗体偶联药Trodelvy,用于治疗既往接受过至少2种疗法的转移性三阴性乳腺癌成人患者;Seattle Genetics与默沙东公司达成肿瘤领域的合作,将在全球范围内联合开发并推广靶向LIV-1的抗体偶联药物ladiratuzumab vedotin。
除了跨国药企以外,许多中国本土创新药企也在有条不紊地探索ADC领域。2022年上半年发布的《2021年度中国抗肿瘤新药临床研究评述》显示,国内外多家药企的该类产品进入临床和临床前阶段,国内布局Trop-2 ADC药物的企业包括复旦张江、上海诗健、科伦药业、百奥泰及君实生物等。正在进行的临床研究有10余项,其中4项为国际多中心研究,4项为III期临床研究,如在既往接受过一线或二线全身化疗的无法手术或转移性激素受体阳性、HER2阴性乳腺癌受试者中比较Dato-DXd与研究者所选化疗的开放、随机化III期研究(TROPION-Breast01)等。
针对ADC药物研发投入火热,管线数量蓬勃增长的情况,有证券机构医药行业分析师对21世纪经济报道指出,随着抗体偶联技术的不断迭代,ADC药物越来越多的潜力将被挖掘。ADC这一领域还有相当多的探索机遇:
一是,ADC是非常好的机制,抗体连接化疗药物,可以把两个经典的、经过多年验证的肿瘤治疗方案整合在一起。但在不同的肿瘤疾病领域,它的靶点生物学特性可能不尽相同。所以,针对不同疾病的生物学特性,靶点还需要进行更多探索和研究。
二是,ADC联合治疗是一个相当重要的治疗策略。比如ADC连接小分子、连接免疫治疗等方面在未来都需要进行探索。
三是,双靶点的bispecific antibody(双特异性抗体)被认为是一大趋势。一个肿瘤细胞上可能有不同的靶点,未来如何把不同靶点的驱动基因双抗能够再连接化疗药物,产生更加大的作用。即如何推动双靶点ADC研究发展也可能是一个趋势。
“医药行业是以科学和研究为积累的行业,更基于对于疾病领域的认知。这也要求入局者通过不断的科研探索,加深对疾病biomarker(生物标志物)和靶点基因组学的认知。”前述分析师说。
聚焦差异化竞争
因此,在ADC行业,更多的探索正在进行中。特别是如今ADC领域已然进入高光时刻,市场需求使得无数企业入局,在一定程度上如何改变扎堆以及行业竞争激烈的情况也成为业内人士关注的重点。
但走出一条差异化路径也并非易事,由于研发和生产技术上的挑战,不少ADC药物研发企业只能一味效仿成功案例,一些研发企业甚至将希望寄托于生产端对端、一站式服务平台。因此,如何在激烈竞争中找到突破口,或者在其他众多靶点中找出一个适合的路径,更是成为每个企业值得思考的问题。
智慧芽发布的《“生物导弹”抗体偶联药洞察报告》显示,从适应症和靶点分布来看,肿瘤是目前聚焦的核心方向。但重心已从血液瘤转向实体瘤,HER2仍然是热门靶点,但新靶点的探索也愈发多样化。
张晓雷介绍,ADC药物研发企业想要走差异化道路,首先可以从靶点或者连接子以及有效载荷方面创新,这些创新都具有产生临床意义上差异化的可能性。同时,对于ADC药物研发企业而言,核心还是要理清楚差异化之处,不一定要在靶点上创新,也可解决技术挑战。即便HER2已是成熟靶点,若能够在连接子和小分子毒素上进行创新,都可能产生差异化的临床治疗效果。
从瓴路市场调研情况来看,中国做ADC的公司有很多,但大多数集中在Her2和Trop-2等几个靶点。由于小分子、抗体这两部分从技术角度来讲,门槛非常低,新靶点出来后使药企“纷至沓来”,很难做出差异化,而且仅凭两三年竞争优势很容易被赶超。所以,从Biotech企业本身来看,一定要进行差异化创新,需要做出全世界“First-in-class”,成为中国最具有价值、投资回报率最高的公司。
“在ADC赛道布局上,每家公司技术平台不太一样,与ADC Therapeutics(专注于开发ADC药物的药物研发公司)合作时,我们是从它的毒素,即payload出发,聚焦PBD(吡咯并苯二氮杂䓬二聚体细胞毒素)研究,PBD这也ADC行业公认毒素最高,而在靶点选择上,我们聚焦的靶点CD19是ADC行业尚未有企业聚焦的靶点。”张晓雷说,PBD毒素非常毒,在血液中起效较快,可对DNA形成“沉痛打击”。但因为剂量控制在较小的范围,可以掌握治疗的平衡点。在适应症的选择上,瓴路也需要区别于其他药企侧重实体瘤,更侧重在血液瘤领域,而从已有的数据可以发现,Loncastuximab tesirine目前在血液瘤领域反应较为理想。
实际上,据21世纪经济报道记者了解,尽管CD19这个靶点本身较为普遍,但目前在ADC领域的开发中尚未有多家企业布局。Loncastuximab tesirine是CD19靶点上的第一个ADC产品,这也符合在研ADC聚焦的方向。智慧芽方面认为,从国内外企业的研发管线来看,ADC药物已成为全球创新药企布局的重点方向,3-5年内或迎来新的高峰;从适应症和靶点分布来看,肿瘤是目前聚焦的核心方向,但重心已从血液瘤转向实体瘤,HER2仍然是热门靶点,但新靶点的探索也愈发多样化。
有临床专家在接受21世纪经济报道记者采访时也表示,ADC的药物研发已经发展到第三代,在疗效上、安全性上存在着一些差异。临床也特别希望有疗效更好、安全性更高的药物上市。
《指导原则》也指出,选择创新靶点时也需要关注,在同一靶抗原不同药物间疗效的差异、同一药物针对不同靶抗原表达状态疗效的差异、最佳给药策略的确定、关注脱靶的安全性风险、联合用药等方面需关注的问题。
做好规避风险战略布局
眼下,ADC药物研发企业想要走差异化道路,除了聚焦差异化外,如何规避风险、如何良性竞争、如何做好战略布局也至关重要。
东北证券研报指出,现阶段ADC药物广泛布局肿瘤领域,从总体来看,本土在研管线总数较少,适应症、靶点分布较为集中,热门靶点HER2占比超过30%。此外,已经有部分企业在探索创新靶点,该类靶点赛道尚未形成明显竞争格局,仍然具有较大的发展潜力。
由于ADC药物研发生产对厂房设备、环境、人员操作都有非常严格的要求,使其使用CDMO服务的比例相较于一般生物药要高得多。因此,包括Seattle Genetics在内的老牌ADC研发公司都通过与CDMO公司合作的形式推进研发过程。这样的方式效率更高,可以使研发企业能够专注于自己擅长的早期研发和临床试验等环节。
一方面,ADC药物的工艺痛点凸显。将大分子跟小分子组合的工艺较为复杂,工艺开发量是传统抗体的2-3倍。且抗体和小分子都要分别有自己完整的工艺,再将它们偶联到一起,分析工作量较大。
另一方面,ADC药物的制剂比较复杂。目前,已经上市的ADC药物主要采用冻干工艺,生物药做成冻干制剂意味着稳定性不够好。然而,之所以要做成冻干,是由于ADC药物既有亲水的成分,又有疏水的成分,在液体的环境很难保持长期稳定。这也是为什么ADC药物的研发生产外包比例要比普通生物药更高,大部分公司都没有能力独立完成整个制作流程。
这也使不少ADC药物研发企业一味效仿成功案例,亦或是不少ADC药物研发企业将希望寄托于生产端对端、一站式服务平台。
此外,通常情况下,ADC药物产业链主要由上游研发企业主导,委托CMO公司专业化生产ADC药物,与CSO公司约定药品销售模式。例如由上游创新药企Seagen研发药物、开发技术;再由CMO公司如ABZENA、Novasep专业化生产ADC药物,药企支付制造与工艺优化费用;在销售环节,Seagen将北美以外地区授权给武田公司获得销售分成。这种产业模式减少了创新企业开发药物的成本,降低了药品生产的风险和难度,也促使各企业之间的合作与交易。
在谈及如何规避ADC市场的潜在风险时,张晓雷提到,“做ADC是否有不一样的技术,是否有不一样的靶点,从企业战略布局上都需要有详细的规划。同时,专业的团队也成为制胜关键,在技术门槛较高的领域,企业需要提升团队运营效率,具备较高的执行能力,以资深、专业的团队配置应对随时而来的市场挑战。”
(作者:季媛媛,实习生洪小澜 编辑:包芳鸣,见习编辑,张铭心)
证券之星财经:
2022年9月23日复旦张江(688505)发布公告称海通证券股份有限公司朱赵明、上海理成资产管理有限公司陈颖、上海睿郡资产管理有限公司吴雨潇、上海莫暮投资管理有限公司吴平于2022年9月21日调研我司。
具体内容如下:
问:按照公司股权激励的目标,公司今年需要达成12亿的营收,上半年疫情对于该目标的达成是否会造成困难?
答:目前公司的股权激励计划制定于2021年,当初制定的激励目标合理。2022年3月起,上海新冠疫情形势严峻给公司业绩造成了一定的影响,直到6月初上海陆续解除全域静态管理,公司经营活动得以逐步恢复。公司已积极采取相应的一系列措施,降低疫情造成的短期影响,并将尽力完成激励计划制定的目标。
问:公司的光动力上市产品艾拉、复美达一次的使用治疗时间?
答:公司光动力技术平台处于世界领先水平,其产品需配合光动力设备使用。一般而言,艾拉配合光动力设备的照光时间依具体 治疗的情况而定,复美达标准剂量在同一光斑照射的时间一般为20分钟/次。
问:公司上市产品艾拉正在进行其拓展适应症的研究试验,进展如何?
答:公司盐酸氨酮戊酸用于治疗宫颈癌前病变的项目,目前正处于II c期临床研究;用于治疗痤疮的适应症研究,目前正在进行II期临床研究;用于治疗光化性角化病的II期临床试验于今年8月完成首例受试者入组,均进展顺利。其中用于治疗痤疮的适应症研究因其临床效果可以比较快速地体现,所以该项目研究的进展相对更快。
问:公司研发管线丰富,涉及多种适应症和科室,在这些研发管线中,是否有侧重推进的项目,公司的研发战略是什么?
答:公司一直以来的研发战略都是从探索临床治疗的缺失和不满意并提供更有效的治疗方案和药物为核心定位出发,针对选定药物拓展新的临床适应症以及针对选定疾病继续拓展新的药物并设计出新的治疗方案的研究模式。其创新性研发领域主要集中在针对皮肤疾病、肿瘤和癌前病变的光动力药物、针对肿瘤的抗体偶联药物、针对帕金森病全方位治疗的缓控释药物。Me-too类药物有针对自身免疫性疾病以及肿瘤的小分子靶向药物等,仿制类药物主要有针对肿瘤的纳米药物,以及拥有专利或技术壁垒的其它药物。自科创板上市以来,公司各个平台的主要研发项目均取得了显著突破基因工程技术平台治疗肿瘤的抗Trop2抗体偶联SN38项目于2021年初获得临床试验受理,同年年中获临床批件,并于年底完成临床研究首例受试者入组;2022年上半年,用于治疗晚期实体瘤的抗Her2抗体偶联BB05项目I期临床试验申请获得受理;光动力技术平台中艾拉(盐酸氨酮戊酸)拓展适应症的研发项目如治疗中重度痤疮的项目于2020年完成I期临床试验并于2021年初进入II期临床阶段、治疗轻中度光角化病的项目于2021年10月获得II期临床试验受理,同时复美达(海姆泊芬)用于治疗鲜红斑痣在美国的II期临床试验申请于2021年底获FD受理;纳米技术平台治疗肿瘤的里葆多(盐酸多柔比星脂质体注射液)一致性评价申请于今年7月获得受理;口服固体制剂平台JK1选择性抑制剂用于治疗中重度特应性皮炎项目及治疗溃疡性结肠炎项目II期临床试验于2021年11月获得受理;治疗原发性胆汁性胆管炎的奥贝胆酸项目于2021年初获得确证性临床试验受理、年中获临床批件并于年底完成临床研究首例受试者入组。
问:公司上市产品艾拉和复美达是否已经到达峰值?
答:作为一个在临床上有独特治疗效果及治疗优势的药品,公司认为艾拉虽已上市十几年,但随着其拓展适应症(如中重度痤疮/光角化病等)的研发进展不断推进,以及光动力药物对于目前临床治疗难点等复杂的疾病所表现出来的优异治疗效果,可以预计艾拉未来的拓展空间会更大。复美达于2017年开始上市销售,上市后的IV期临床研究也在持续推进中成人安全性研究已结束,正处于数据收过程中,儿童安全性研究,已完成7-14岁研究,2-7岁尚缺2例,待全部研究结束后,数据将公开。复美达最有治疗意愿的受众是儿童,基于安全性的考虑,公司在整个推广过程中秉承审慎的态度。未来,随着上市后研究的完成,会适时调整推广策略。相信随着其在中国的深入推广及全球注册的推进,该产品未来的拓展空间很大。
问:受上海上半年疫情影响,公司光动力产品销售下降,是生产端的原因还是渠道端的原因?终端库存是否存在断货情况?
答:公司上半年上海疫情期间未发生断货情况,不影响终端。公司光动力产品的销售下降更多是因为疫情封控地区生产经营、物流管控等原因导致销售收入下降。
问:请进一步介绍一下公司药物的研发投入以及研发人员情况?
答:公司先进的经营理念和激励制度吸引了大批的技术人才加入公司,形成了成熟的研发技术团队,这些技术团队即是公司核心技术平台的载体。公司2019年至2021年度研发投入总额分别为1.28亿、1.39亿、2.48亿,2020年科创板上市以来研发投入占营业收入比重明显增长。截至2022年6月30日,公司研发人员总数为151人,较去年同期增长18.89%。研发人员普遍高学历,人才引进方式多元、专业构成多元。
问:公司对于自身区别于其他药物研发企业的优劣势是?
答:公司光动力技术已处于世界领先水平,已上市产品艾拉(全球首个针对尖锐湿疣的光动力药物)填补了特殊部位尖锐湿疣治疗的国际空白,成为国内光动力治疗的代表性产品;已上市产品复美达(全球首个针对鲜红斑痣的光动力药物)有着化合物结构稳定、光毒作用低、代谢迅速、避光期短、病灶消退均匀、治愈率高、瘢痕发生率低、不易复发等显著优势;基因工程技术平台中第一个DC药物,即治疗肿瘤的注射用重组人鼠嵌合抗CD30单克隆抗体-MCC-DM1偶联剂是一次DM1技术于DC项目中在CD30靶点上的探索,该药物作为全新化合物,其研发处于国际领先水平。同时,近年来,公司在小分子端构建的全新BB05linker-drug平台已公开了一项mb-BB05DC药物的专利,其在体外血浆稳定性、体外释放/旁观者效应、体内PK/PD方面,与已经批准上市的原研产品高度一致,这为集团后续开发Me-better或创新DC药物奠定了基础;纳米技术平台中已上市产品里葆多是一种采用先进的隐形脂质体技术包封,具有被动靶向特性的多柔比星新剂型。它是蒽环类药物的更新换代产品,在肿瘤治疗学上具有提高疗效、降低心脏毒性、骨髓抑制以及减少脱发等优势;口服固体制剂平台中正在研发的小分子靶向药物JK1选择性抑制剂,作为口服JK制剂在临床研究中亦表现出了让人惊艳的效果,同时在起效时间和使用方式上具有天然的优势;公司与汉都医药合作的针对早期帕金森病的卡左双多巴控释片项目(WD-1603)项目采用汉都医药的专利技术平台UGi-Pump技术,使左旋多巴剂型在胃肠道上段滞留时间延长,且在滞留时间里,持续稳定地释放药物,从而获得稳定的血药浓度,很大程度地推迟帕金森病进程,降低药物引起的不良反应。公司始终坚持以探索临床治疗的缺失和不满意并提供更有效的治疗方案和药物为核心定位,以新药研发为立足之本和使命,务求成为生物医药业界的创新者及领先者。这样的立项宗旨使得目前公司已上市的产品和在研项目都表现出很好的发展前景和受政策变化影响较小的特点,奠定了公司在新政策环境下发展的基础和动力。同时,公司亦正在开发若干从提高生物利用度、改良剂型等方面入手,拥有专利或工艺壁垒的仿制药物,以帮助本集团进一步丰富研发管线,缩短新产品上市周期,有效利用研发及产能资源,实现经济效益的最大化。公司从项目筛选、到立项、再顾、最终上市销售,这是一个不断推出新技术和新产品的创新与整合资源的过程,也因此形成了公司在市场上独特的竞争优势。
问:公司位于泰州的工厂,其产能利用率是?
答:目前只有复美达、帕瑞昔布钠的生产线在泰州复旦张江工厂,因此产能利用率目前仅约20%。
问:公司海姆泊芬化合物的专利申请是在2006年,是否会对其境内的销售及海外申报进程造成影响?
答:海姆泊芬及注射用海姆泊芬(商品名复美达)于2017年上市销售,公司拥有海姆泊芬及注射用海姆泊芬相关专利累计12项,现在有效期内的发明专利4项,其专利保护到期时间分别为2023年、2024年、2026年,另有数项正在审查中的发明专利申请。公司光动力技术处于世界领先水平,多年来持续拓展基于光动力技术平台的药物研发及疾病治疗方案。公司光动力药物主要为治疗尖锐湿疣的艾拉和治疗鲜红斑痣的复美达,目前均为国内独家生产销售产品。公司一直重视构建对现有产品和研发项目的专利保护,定期维护现在有效期内的相关专利,并及时拓展申报新专利,以此延长产品及项目的生命周期。根据过往的销售情况而言,部分即将到期的相关专利对公司现有产品的销售不会产生影响。
复旦张江主营业务:主要从事生物医药的创新研究开发、生产制造和市场营销
复旦张江2022中报显示,公司主营收入2.71亿元,同比下降32.02%;归母净利润-3597.45万元,同比下降154.94%;扣非净利润-4561.85万元,同比下降183.64%;其中2022年第二季度,公司单季度主营收入1.3亿元,同比下降52.19%;单季度归母净利润-4090.04万元,同比下降167.75%;单季度扣非净利润-4628.44万元,同比下降184.01%;负债率21.44%,投资收益587.98万元,财务费用-184.97万元,毛利率89.62%。
该股最近90天内无机构评级。融资融券数据显示该股近3个月融资净流出79.08万,融资余额减少;融券净流入148.43万,融券余额增加。根据近五年财报数据,证券之星估值分析工具显示,复旦张江(688505)行业内竞争力的护城河一般,盈利能力一般,营收成长性良好。财务相对健康,须关注的财务指标包括:应收账款/利润率。该股好公司指标3星,好价格指标1.5星,综合指标2星。(指标仅供参考,指标范围:0 ~ 5星,最高5星)
以上内容由证券之星根据公开信息整理,与本站立场无关。证券之星力求但不保证该信息(包括但不限于文字、视频、音频、数据及图表)全部或者部分内容的的准确性、完整性、有效性、及时性等,如存在问题请联系我们。本文为数据整理,不对您构成任何投资建议,投资有风险,请谨慎决策。
复旦张江(SH688505):
复旦张江2022年9月投资者关系活动记录表 网页链接
复旦张江(SH688505):
复旦张江:复旦张江2022年9月投资者关系活动记录表 网页链接
北亚:
复旦张江(SH688505)
微芯生物(SH688321)
科伦药业(SZ002422)
相比之下,复旦张江可能预期差最大
宽客-顺势天成:
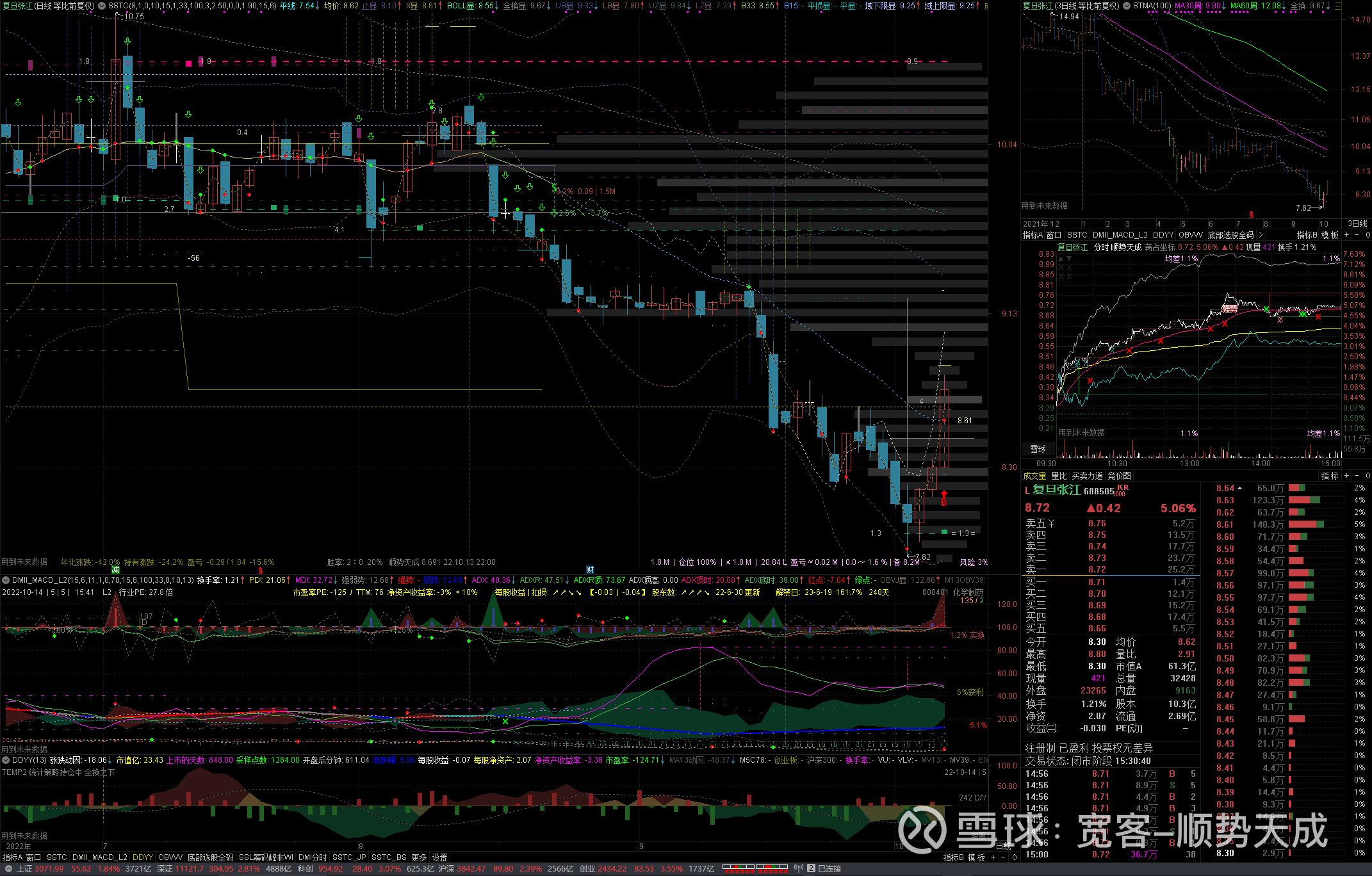
复旦张江(SH688505)
锈铁点金:
复旦张江(SH688505) 复旦张江的帕金森病,临床三期,进展的怎么样?有谁知道?非常感谢!!
股票
MORE>- 最近发表
- 标签列表
-
-
SZ002799 SH603203 SZ000046 SZ002182 SH605016 SH600888 SH600584 SZ003020 SH600599 SZ002701 SH603219 SH603871 SZ002672 SZ002463 SH600692 SZ300417 SZ002510 SH601838 SH603133 SZ300977 SZ002842 SZ300985 SH688095 SZ000009 SZ002686 SZ000413 SZ300232 SZ000901 SZ300940 SZ300537 SZ002760 SH603500 SH603816 SZ301258 SH603018 SZ002773 SH688381 SZ300340 SZ002569 SH688190 SZ002438 SZ300385 SZ002751 SH688779 SZ002348 SZ300093 SH600552 SZ300131 SZ300382 SZ002458

